药闻播报 | 2月26日-3月2日热点信息汇总→

各位同仁,周一愉快!
小诺为您汇总了上周的热点药闻
👉1、《中华人民共和国保守国家秘密法》已由中华人民共和国第十四届全国人民代表大会常务委员会第八次会议于2024年2月27日修订通过,自2024年5月1日起施行。
👉2、国务院总理李强3月1日主持召开国务院常务会议,审议通过《推动大规模设备更新和消费品以旧换新行动方案》,研究加快现代化基础设施体系建设、持续深入推进长三角一体化高质量发展等工作,讨论《〈中华人民共和国农业技术推广法〉等3部法律的修正案(草案)》。
👉3、国务院关于《重庆市国土空间总体规划(2021—2035年)》的批复。
👉4、工业和信息化部等七部门关于加快推动制造业绿色化发展的指导意见。
👉5、工业和信息化部关于印发《工业领域数据安全能力提升实施方案(2024-2026年)》的通知。
👉6、工业和信息化部 国家发展和改革委员会 财政部 国家税务总局关于开展2023年度享受研发费用加计扣除政策的工业母机企业清单制定工作的通知。
👉7、国家发展改革委 财政部 税务总局关于印发《海南自由贸易港鼓励类产业目录(2024年本)》的通知。
👉8、专利文献馆2024年3月公益讲座计划:“专利业务办理及系统使用”专题。
👉9、国家中医药管理局科技司关于公开征集国家重点研发计划“中医药现代化”重点专项2024年度项目建议的通知。
👉10、国家中医药管理局关于组织开展全国中医药经济管理领军人才第一期学员选拔培养工作的通知。
👉11、国家中医药管理局拟新增全国中医药文化宣传教育基地名单公示。
👉12、人力资源社会保障部办公厅 国家医疗保障局办公室关于颁布健康照护师(长期照护师)国家职业标准的通知。


国家药监局及直属单位药品相关数据2月26日-3月2日
☆一、NMPA(国家药品监督管理局)政策文件发布征求新闻类:
★1、国家药监局综合司关于同意北京市药品检验研究院调整生物制品批签发证明文件授权签发人的复函。
★2、国家药监局综合司关于同意广东省药品检验所调整生物制品批签发证明文件授权签字人的复函。
★3、国家药监局综合司关于同意江苏省食品药品监督检验研究院调整生物制品批签发证明文件授权签发人的复函。
★4、全国中药注册管理和质量安全监管工作会议召开。
★5、2024年国家药品抽检工作会召开。
★6、李利会见以色列驻华大使潘绮瑞。
★7、徐景和在北京调研医疗手术机器人产业发展和质量监管工作。
★8、雷平在海南调研化妆品产业创新发展和监管工作。
★9、徐景和在河北调研加强省级医疗器械审评审批能力建设工作。
☆二、NMPA(国家药品监督管理局)信息公示类
▲1、上市批准信息公示:
△新药上市批准信息公示:本周无。
△新医疗器械上市批准信息公示: 颅内动脉瘤CT造影图像辅助检测软件获批上市
△其他上市信息公示:本周无。
▲2、仿制药参比制剂目录发布信息:本周无新增,共计发布七十七批。
▲3、说明书修订信息: 本周无。
▲4、药品批准证明文件送达信息发布:
△2024年2月26日
△2024年2月27日
△2024年3月1日
▲5、药品通知件待领取信息发布:
△2024年2月26日
△2024年2月27日
△2024年2月28日
△2024年3月1日
▲6、中药品种保护信息公示:初保:小儿感冒舒颗粒、黄厚止泻滴丸、抗狼疮散
▲7、药品注册证书注销、暂停进口信息:本周无。
▲8、补充检验方法信息:本周无。
▲9、药品—常见问题列表:本周无新增,共计发布79条
☆三、CDE(国家药品监督管理局药品审评中心)药品技术指导原则、指南发布类征求新闻类:
◆ 1、国家药监局药审中心关于在中国上市药品专利信息登记平台设置法律文书提交模块的通知
◆ 2、关于更新电子申报资料制作软件的通知
◆ 3、国家药监局药审中心关于发布《中药制剂特征图谱研究技术指导原则(试行)》《中药制剂稳定性研究技术指导原则(试行)》的通告(2024年第16号)
◆ 4、国家药监局药审中心关于发布《生长激素制剂用于生长激素缺乏症临床试验技术指导原则》的通告(2024年第18号)
◆ 5、国家药监局药审中心关于发布《小儿便秘中药新药临床研发技术指导原则(试行)》的通告(2024年第19号)
☆四、CDE(国家药品监督管理局药品审评中心)新承办信息公示类:
■1、境内企业新药申报承办情况统计:
■2、进口申报承办情况统计:
■3、境内企业仿制药申报承办情况统计:
■4、化药一致性评价申报承办情况统计:
□(1)国内未改变处方工艺的一致性评价申请或提出免于参加一致性评价的申请:本周无。
□(2)进口未改变处方工艺的一致性评价申请或提出免于参加一致性评价的申请:本周无。
□(3)国内改变处方工艺的一致性评价:
□(4)进口改变处方工艺的一致性评价:本周无。
■5、原料药登记信息公示:
■6、药用辅料登记信息公示:
■7、药包材登记信息公示:
☆五、CDE(国家药品监督管理局药品审评中心)信息公示类:
●1、临床试验默示许可:新增96条,共计12871条
●2、优先审评公示
○(1)拟优先审评品种公示:盐酸安罗替尼胶囊、肾上腺素注射液(预充式)、己二酸他雷替尼胶囊(Taletrectinib Adipate Capsules)
○(2)纳入优先审评品种:Belzutifan片、Vamorolone口服混悬液
○(3)异议论证结果查询:本周无。
●3、突破性治疗公示
○(1)拟突破性治疗品种公示:PM8002注射液、注射用SKB264、纳武利尤单抗注射液、伊匹木单抗注射液
○(2)纳入突破性治疗品种:本周无。
○(3)异议论证结果查询:本周无。
●4、《化学仿制药参比制剂目录》的公示:本周无新增,第七十九批公示期限:2024年02月21日~2024年03月5日(10个工作日),公示共计七十九批。
●5、共性问题:
○(1)受理共性问题:本周无新增,发布共计65条
○(2)常见一般性技术问题:本周无新增,发布共计213条,其中重复发布了22条
○(3)化学仿制药共性问题:本周无新增,发布共计28条
●6、仿制药质量和疗效一致性评价百问百答:本周无新增,共计3期41个问答
●7、eCTD专栏 >> 常见问答:本周无新增,共计15条
●8、上市药品信息:本周无新增,信息公示共计1230条。
☆六、CMDE(国家药品监督管理局医疗器械技术审评中心)发布公示信息:本周无。
☆七、NMPAIC(国家药品监督管理局信息中心)发布公示信息:本周无。
☆八、CFDI(国家药品监督管理局食品药品审核查验中心)发布公示信息:本周无。
☆九、CHP(国家药典委员会)发布公示信息:
§ 国家药典委员会2024年度国家药品标准提高课题拟立项目录公示
☆十、NIFDC(中国食品药品检定研究院)发布公示信息:
∮1、中检院公开征求《药品注册检验工作程序和技术要求规范(修订草案征求意见稿)》意见的通知
∮2、关于征集细菌和病毒等病原体数字PCR定量检测能力比对研究单位的通知
☆十一、CDR-ADR(国家药品监督管理局药品评价中心-国家药品不良反应监测中心)发布公示信息:本周无。
☆十二、CFE-SAMR(国家市场监督管理总局食品审评中心(国家中药品种保护审评委员会))发布公示信息:本周无。
☆十三、CNCSDR(中国药品监督管理研究会)发布公示信息:本周无。
☆十四、CCFDIE(中国食品药品国际交流中心)发布公示信息:
⊙ 关于第十四届中国医疗器械监督管理国际会议(CIMDR) 参展事宜告知书


中国上市药品专利信息登记平台数据信息
(2-26至3-1)
中国上市药品专利信息登记平台
专利信息公示
中药专利信息本周无新增公示,共计370条
化药专利信息本周无新增公示,共计914条
生物制品专利信息本周无新增公示,共计164条
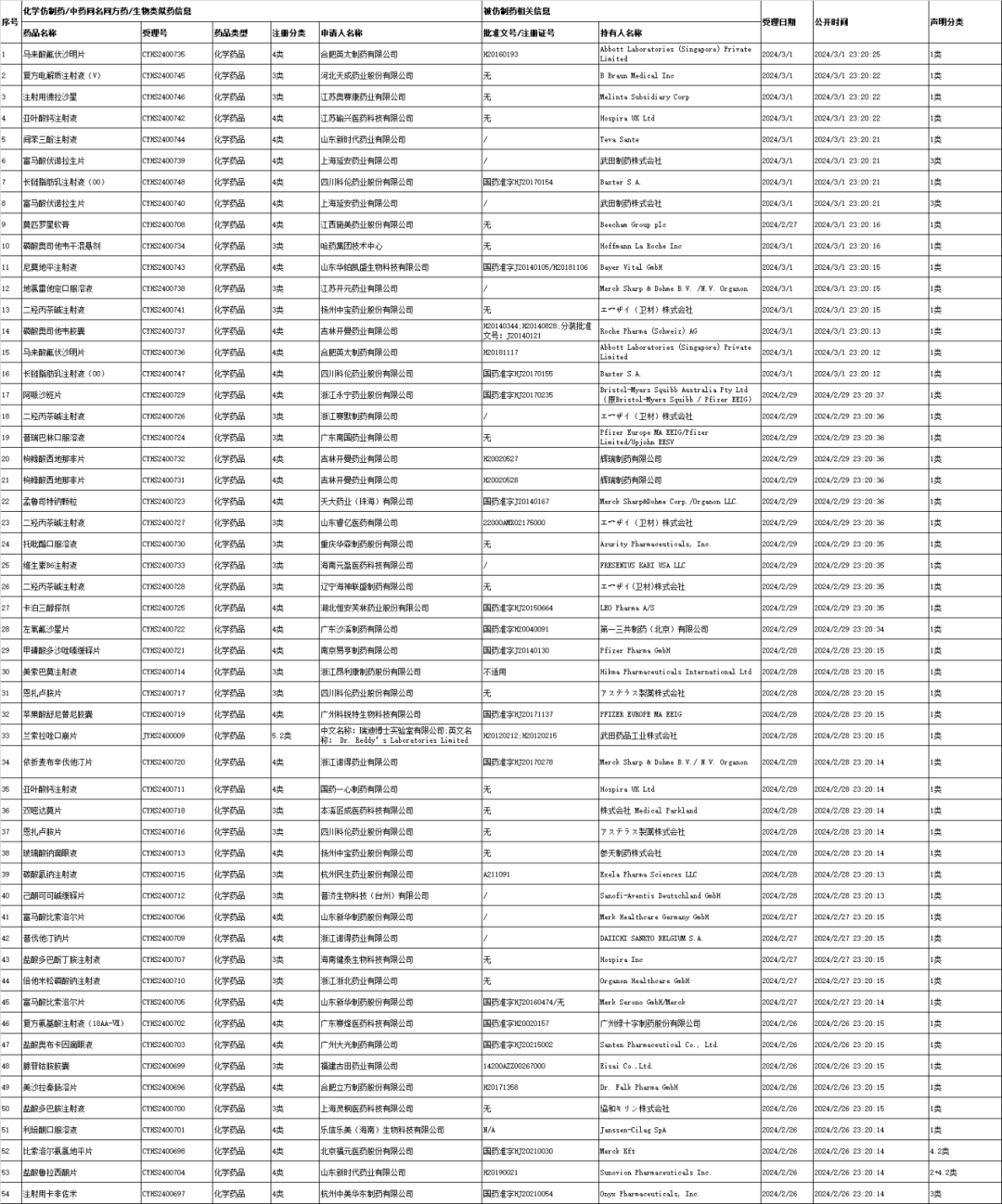
专利声明列表
本周新增公示54条,实际显示公示共计8066条