国家药监局及直属单位药品相关数据信息一周集锦 (2023-01-08至2023-01-14)


1月6日,阳光诺和为期一个月的「守护生命 网购新冠进口药真伪检测公益行动」正式开启。我们针对Paxlovid(奈玛特韦片/利托那韦片组合包装)和Lagevrio-Molnupiravir(莫诺拉韦胶囊)两款非原研的进口仿制「药品」提供免费检测。 截至目前,公益检测行动仍在进行中,也希望大家能继续转发活动,让此次公益行动走得更远。但需要注意的是,阳光诺和只接收奈玛特韦、莫诺拉韦这两个成分的样品的邮寄检测(暂不提供利托那韦片的检测)。
目 录
一
NMPA政策文件发布征求类:
-
国家药监局关于印发进一步加强中药科学监管促进中药传承创新发展若干措施的通知
-
国家药品监督管理局行政受理服务大厅关于2023年春节放假安排的公告(第323号)
-
2022第十六届中国制药工程大会召开
-
焦红在河北调研新冠疫情防控药品保质保供工作
-
李利在核查中心调研时强调 全面强化监督检查 切实保障防疫药械质量安全
-
赵军宁出席中药用于新冠病毒感染治疗临床优势及疗效评价专家座谈会
-
徐景和在安徽江苏调研新冠疫情防控药品医疗器械监管工作
-
黄果在京调研新冠疫苗药物研发进展
二
NMPA信息公示类:
-
上市批准信息公示:
(1)新药上市批准信息公示:附条件批准琥珀酸莫博赛替尼胶囊
(2)新医疗器械上市批准信息公示:本周无。
(3)其他上市信息公示:本周无。
-
仿制药参比制剂目录发布信息:本周新增第六十三批,共计发布六十三批。
-
说明书修订信息:伊班膦酸钠注射液、胸腺肽注射剂
-
药品批准证明文件送达信息发布:
(1)2023年1月9日
(2)2023年1月11日
(3)2023年1月13日
-
药品通知件待领取信息发布:
(1)2023年1月9日
-
药品批准证明文件(纠错)待领取信息:本周无。
-
中药品种保护信息公示:追风透骨胶囊(初保)、芪麝丸(续保)
-
药品注册证书注销、暂停进口信息:本周无。
-
补充检验方法信息:本周无。
三
CDE药品技术指导原则、指南发布类征求类:
本周无。
四
CDE新承办信息公示类:
-
境内企业新药申报承办情况统计:
-
进口申报承办情况统计:
-
境内企业仿制药申报承办情况统计:
-
化药一致性评价申报承办情况统计:
(1)国内未改变处方工艺的一致性评价申请或提出免于参加一致性评价的申请:
(2)进口未改变处方工艺的一致性评价申请或提出免于参加一致性评价的申请:本周无。
(3)国内改变处方工艺的一致性评价:
(4)进口改变处方工艺的一致性评价:本周无。
-
原料药登记信息公示:
-
药用辅料登记信息公示:本周无
-
药包材登记信息公示:
五
CDE信息公示类:
-
临床试验默示许可:新增71条,共计9107条
-
优先审评公示
(1)拟优先审评品种公示:注射用舒巴坦钠/注射用度洛巴坦钠组合包装、西达基奥仑赛注射液
(2)纳入优先审评品种:本周无。
(3)异议论证结果查询:本周无。
-
突破性治疗公示
(1)拟突破性治疗品种公示:Donanemab注射液
(2)纳入突破性治疗品种:本周无。
(3)异议论证结果查询:本周无。
-
《化学仿制药参比制剂目录》的公示:本周新增第六十六批,公示期限:2023年1月9日~2023年1月20日(10个工作日),公示共计六十六批。
(1)化学仿制药尚未发布参比制剂目录(第六十六批)(征求意见稿)
(2)已发布化学仿制药参比制剂增补目录(征求意见稿)
(3)未通过审议品种目录
-
共性问题:
(1)受理共性问题:本周无新增,共计36条
(2)常见一般性技术问题:本周新增10条,共计159条
-
仿制药质量和疗效一致性评价百问百答:本周无新增,共计3期41个问答
-
eCTD专栏 >> 常见问答:本周无新增,共计15条
-
上市药品信息:本周无新增,信息公示共计1024条
六
CMDE发布公示信息:
本周无
七
NMPAIC发布公示信息:
本周无
八
CFDI发布公示信息:
本周无。
九
CHP发布公示信息:
-
关于转发第一批国家中药饮片炮制规范的通知
-
标准公示——滴点测定法标准草案的公示、药包材环氧乙烷测定法标准草案的公示、消石片国家药品标准草案的公示
十
NIFDC发布公示信息:
本周无。
十一
CDR-ADR发布公示信息:
本周无。
(1)非处方药转换阿胶胶囊和柴黄口服液的公示
十二
CFE-SAMR发布公示信息:
本周无。
十三
CNCSDR发布公示信息:
-
课题系列报道 ▏2022年度研究会立项课题结题会:《医疗器械监管职业化专业化人才培养体系的研究——以医疗器械检查员为例》
-
国家药监局委托课题系列报道 ▏2022年度研究会立项课题结题会:《国家药监局监管科学研究基地发展规划与考核评估研究》
一
NMPA政策文件发布征求类:
1、国家药监局关于印发进一步加强中药科学监管促进中药传承创新发展若干措施的通知
链接:
https://www.nmpa.gov.cn/xxgk/fgwj/gzwj/gzwjyp/20230103172324162.html

2、国家药品监督管理局行政受理服务大厅关于2023年春节放假安排的公告(第323号)

3、2022第十六届中国制药工程大会召开

4、焦红在河北调研新冠疫情防控药品保质保供工作

5、李利在核查中心调研时强调 全面强化监督检查 切实保障防疫药械质量安全

6、赵军宁出席中药用于新冠病毒感染治疗临床优势及疗效评价专家座谈会


7、徐景和在安徽江苏调研新冠疫情防控药品医疗器械监管工作

8、黄果在京调研新冠疫苗药物研发进展

二
NMPA信息公示类:
1、上市批准信息公示:
(1)新药上市批准信息公示:附条件批准琥珀酸莫博赛替尼胶囊
(2)新医疗器械上市批准信息公示:本周无。
(3)其他上市信息公示:本周无。
2、仿制药参比制剂目录发布信息:本周新增第六十三批,共计发布六十三批。

链接:
https://www.nmpa.gov.cn/xxgk/ggtg/qtggtg/20230109160046111.html

3、说明书修订信息:伊班膦酸钠注射液、胸腺肽注射剂

链接:
https://www.nmpa.gov.cn/xxgk/ggtg/ypshmshxdgg/20230109101523165.html

链接:
https://www.nmpa.gov.cn/xxgk/ggtg/ypshmshxdgg/20230109101705181.html

4、药品批准证明文件送达信息发布:
(1)2023年1月9日
2022年11月1日起,行政相对人可登录网上办事大厅的法定代表人空间查看电子证照,按照法人空间内相关提示自行打印。

(2)2023年1月11日
2022年11月1日起,行政相对人可登录网上办事大厅的法定代表人空间查看电子证照,按照法人空间内相关提示自行打印。

(3)2023年1月13日
2022年11月1日起,行政相对人可登录网上办事大厅的法定代表人空间查看电子证照,按照法人空间内相关提示自行打印。
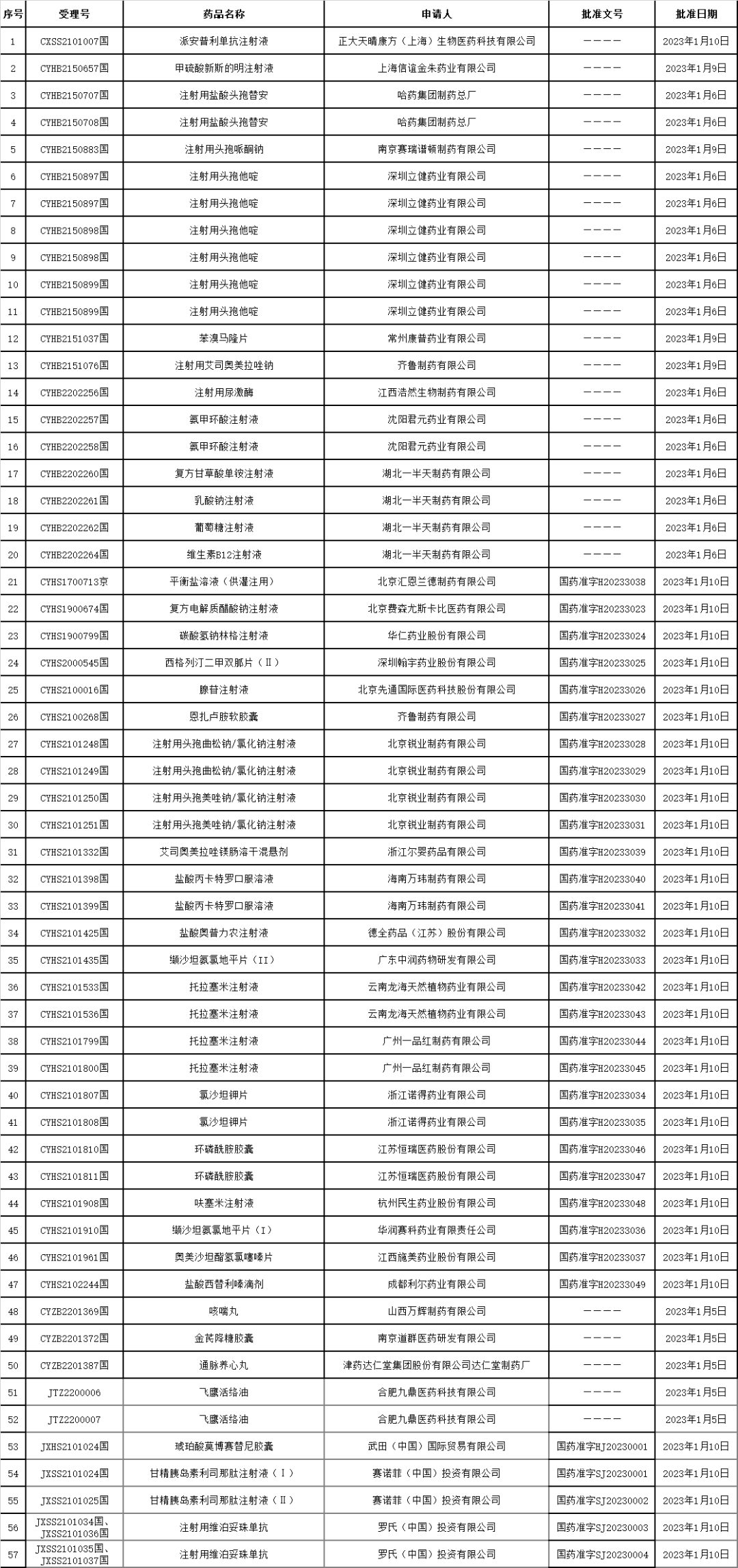
5、药品通知件待领取信息发布:
(1)2023年1月9日

6、药品批准证明文件(纠错)待领取信息:本周无。
7、中药品种保护信息公示:追风透骨胶囊(初保)、芪麝丸(续保)

8、药品注册证书注销、暂停进口信息:本周无。
9、补充检验方法信息:本周无。
三
CDE药品技术指导原则、指南发布类征求类:
本周无
四
CDE新承办信息公示类:
1、境内企业新药申报承办情况统计:

2、进口申报承办情况统计:
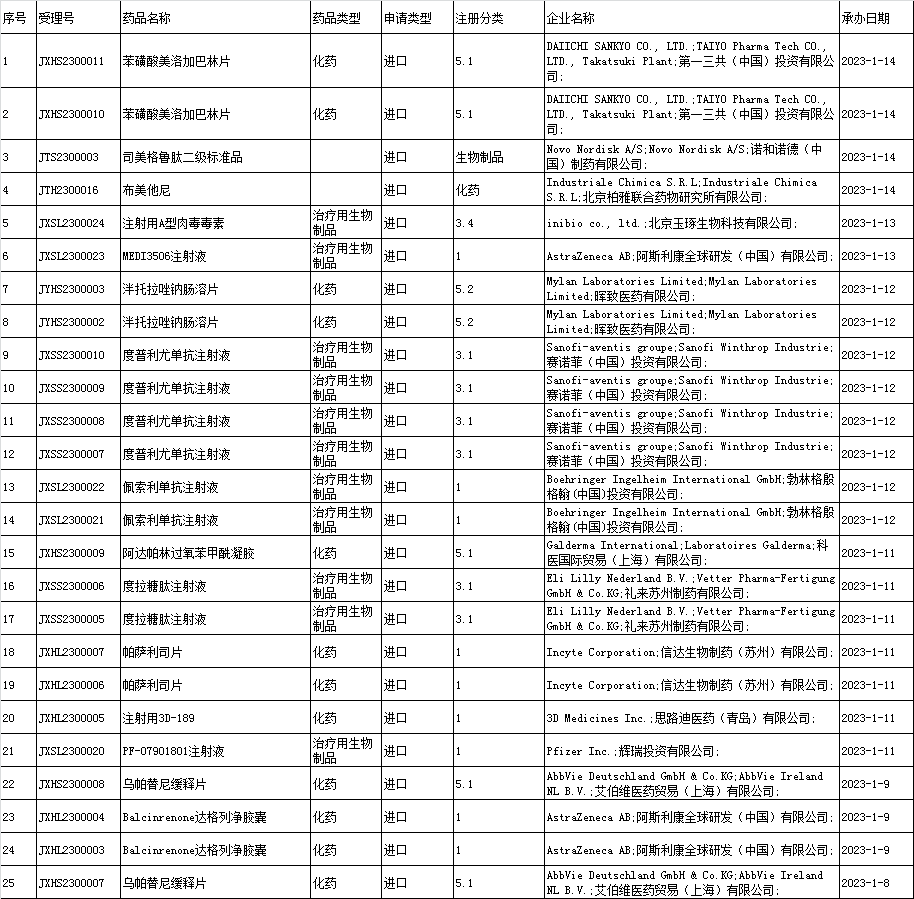
3、境内企业仿制药申报承办情况统计:
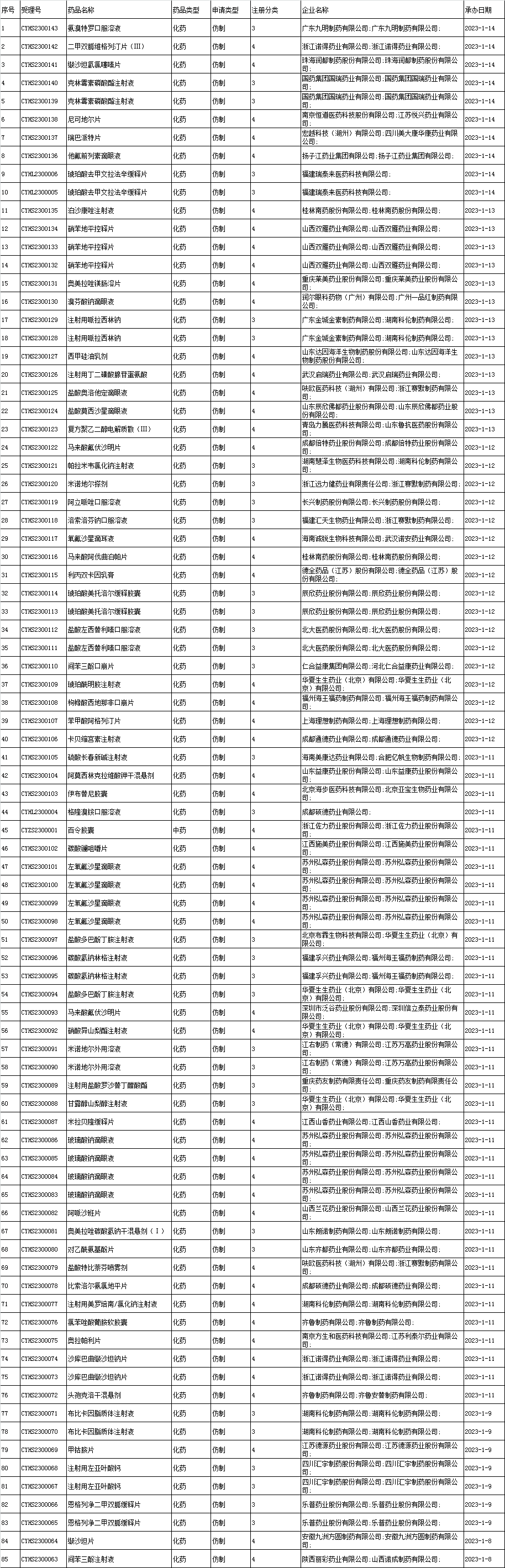
4、化药一致性评价申报承办情况统计:
(1)国内未改变处方工艺的一致性评价申请或提出免于参加一致性评价的申请:

(2)进口未改变处方工艺的一致性评价申请或提出免于参加一致性评价的申请:本周无。
(3)国内改变处方工艺的一致性评价:
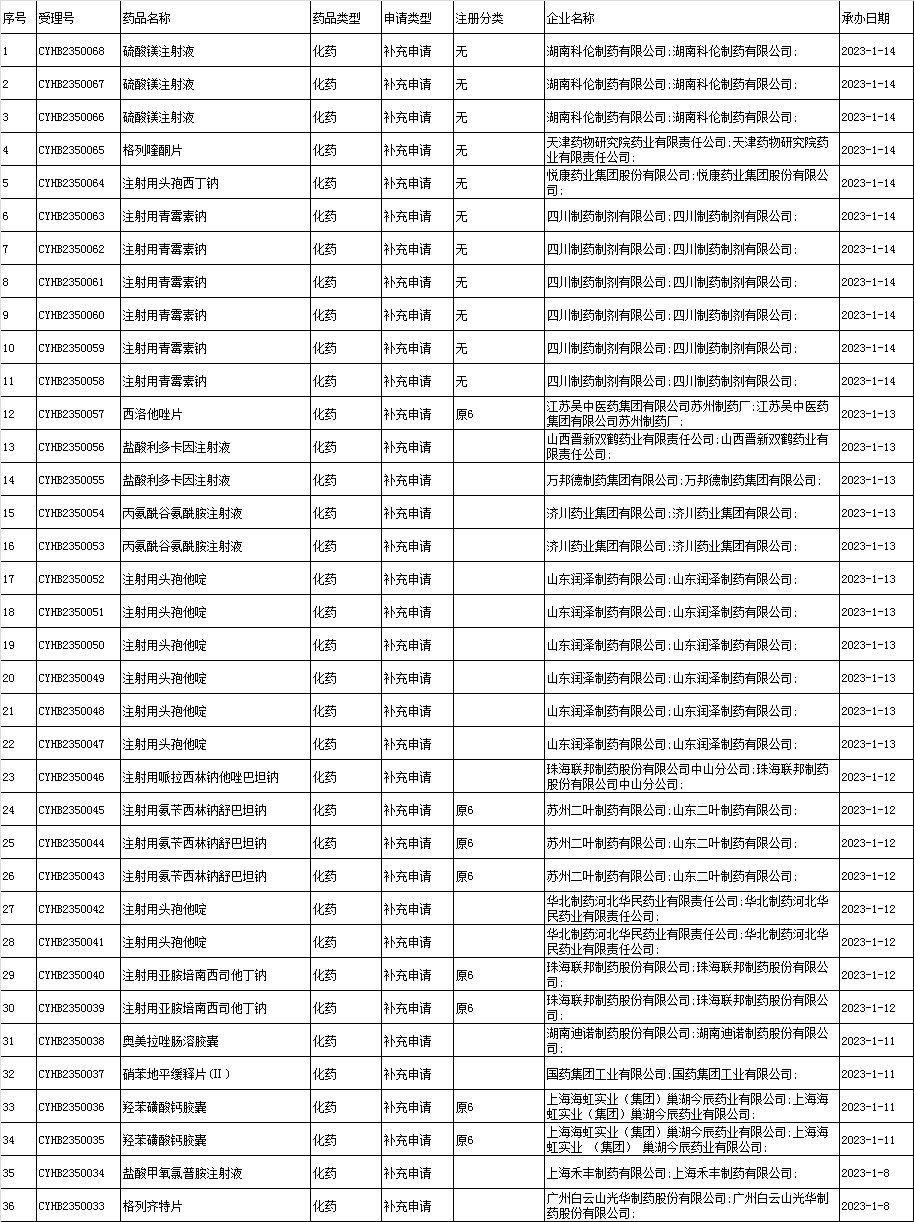
(4)进口改变处方工艺的一致性评价:本周无。
5、原料药登记信息公示:

6、药用辅料登记信息公示:本周无。
7、药包材登记信息公示:

五
CDE信息公示类:
1、临床试验默示许可:新增71条,共计9107条

2、优先审评公示
(1)拟优先审评品种公示:注射用舒巴坦钠/注射用度洛巴坦钠组合包装、西达基奥仑赛注射液

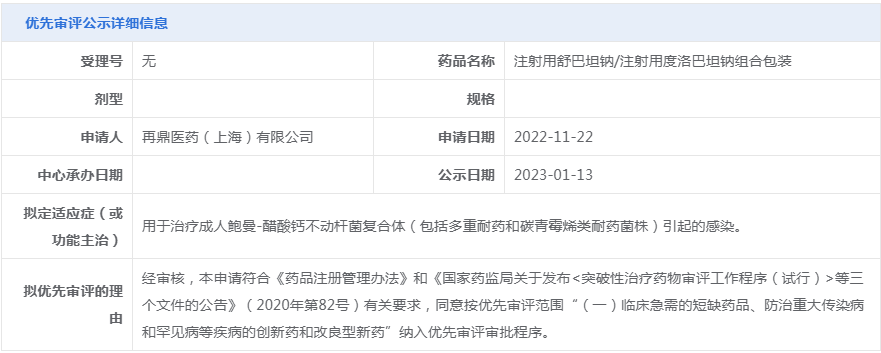

(2)纳入优先审评品种:本周无。
(3)异议论证结果查询:本周无。
3、突破性治疗公示
(1)拟突破性治疗品种公示:Donanemab注射液

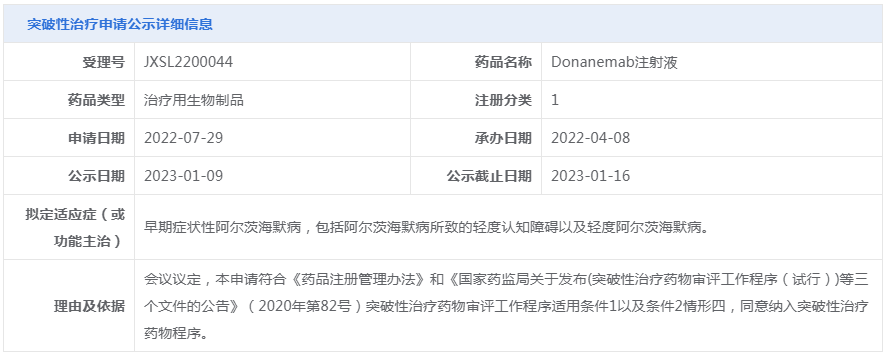
(2)纳入突破性治疗品种:本周无。
(3)异议论证结果查询:本周无。
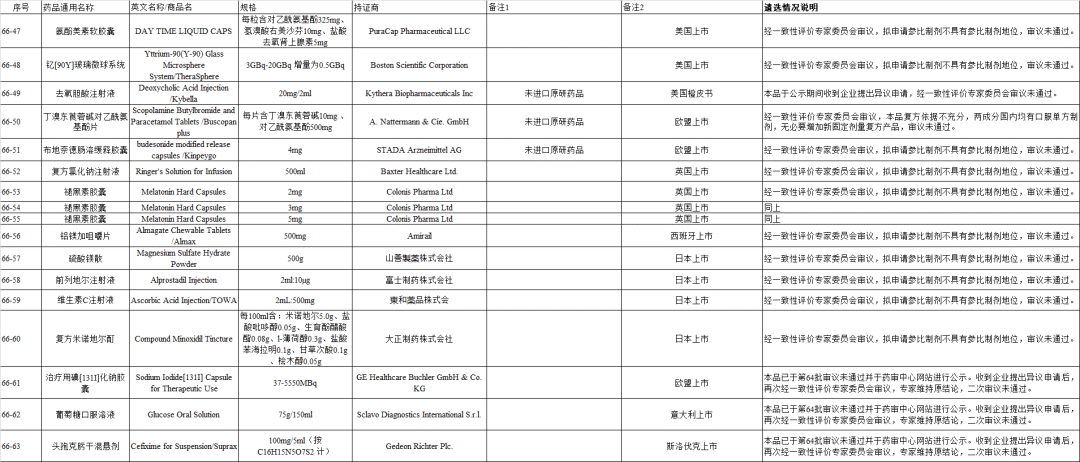
4、《化学仿制药参比制剂目录》的公示:本周新增第六十六批,公示期限:2023年1月9日~2023年1月20日(10个工作日),公示共计六十六批。

链接:
https://www.cde.org.cn/main/news/viewInfoCommon/2ed80bb51cd2598de7359c040b18f31e

(1)化学仿制药尚未发布参比制剂目录(第六十六批)(征求意见稿)


(2)已发布化学仿制药参比制剂增补目录(征求意见稿)


(3)未通过审议品种目录
5、共性问题:
(1)受理共性问题:本周无新增,共计36条
(2)常见一般性技术问题:本周新增10条,共计159条

6、仿制药质量和疗效一致性评价百问百答:本周无新增,共计3期41个问答
7、eCTD专栏 >> 常见问答:本周无新增,共计15条
8、上市药品信息:本周无新增,信息公示共计1024条
六
CMDE发布公示信息:
本周无
七
NMPAIC发布公示信息:
本周无
八
CFDI发布公示信息:
本周无。
九
CHP发布公示信息:
1、关于转发第一批国家中药饮片炮制规范的通知
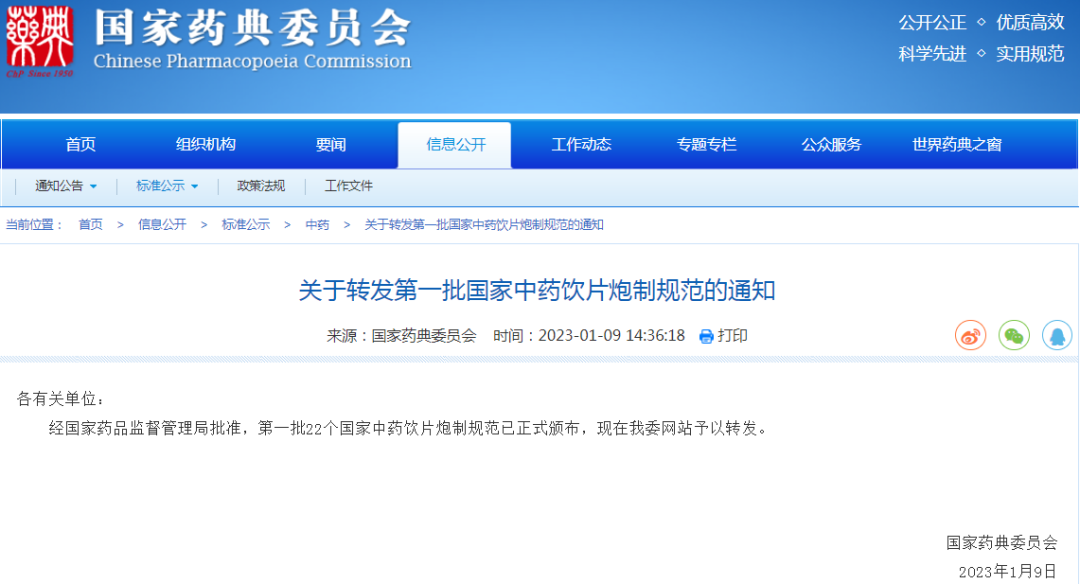

链接:
https://www.chp.org.cn/gjyjw/zy/17555.jhtml

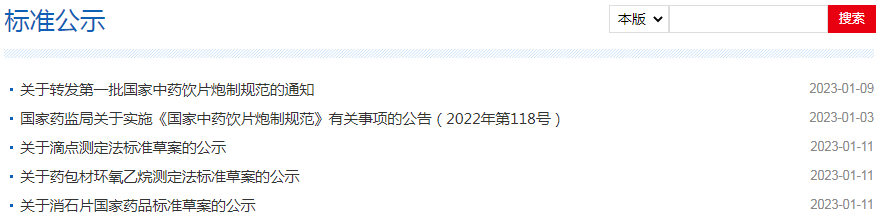
2、标准公示——滴点测定法标准草案的公示、药包材环氧乙烷测定法标准草案的公示、消石片国家药品标准草案的公示
十
NIFDC发布公示信息:
本周无。
十一
CDR-ADR发布公示信息:
本周无。
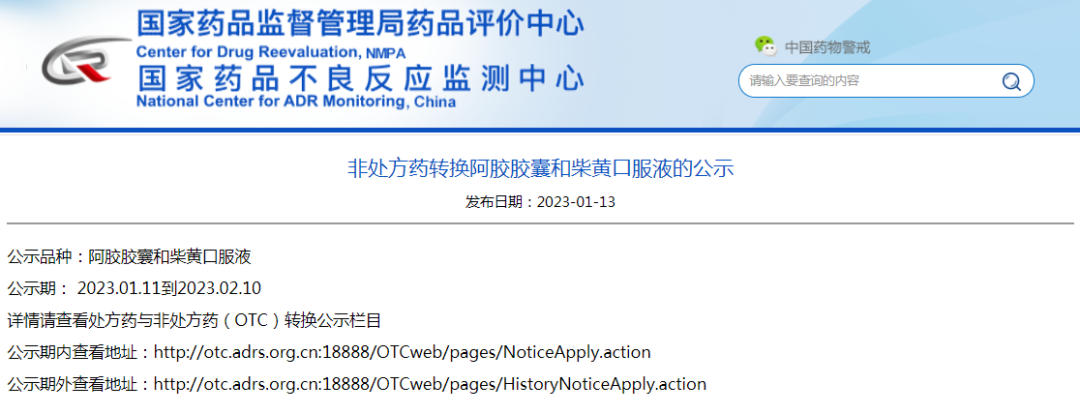
(1)非处方药转换阿胶胶囊和柴黄口服液的公示

十二
CFE-SAMR发布公示信息:
本周无。
十三
CNCSDR发布公示信息:
1、课题系列报道 ▏2022年度研究会立项课题结题会:《医疗器械监管职业化专业化人才培养体系的研究——以医疗器械检查员为例》

2、国家药监局委托课题系列报道 ▏2022年度研究会立项课题结题会:《国家药监局监管科学研究基地发展规划与考核评估研究》