国家药监局及直属单位药品相关数据信息一周集锦(2022-09-12至2022-09-17)

目录
☆一、NMPA政策文件发布征求类:
★1、国家药监局关于批准注册210个医疗器械产品公告 (2022年8月) (2022年第78号)
★2、国家药监局关于17批次药品不符合规定的通告(2022年第43号)
☆二、NMPA信息公示类
▲1、上市批准信息公示:
△新药上市批准信息公示:广金钱草总黄酮胶囊
△新医疗器械上市批准信息公示:本周无。
△其他上市信息公示:本周无。
▲2、仿制药参比制剂目录发布信息:本周新增第五十八批,共计发布五十八批。
▲3、说明书修订信息:本周无。
▲4、药品批准证明文件待领取信息发布:
△2022年9月15日
▲5、药品通知件待领取信息发布:
△2022年9月14日
▲6、药品批准证明文件(纠错)待领取信息:本周无。
▲7、中药品种保护信息公示:本周无。
▲8、药品注册证书注销、暂停进口信息:本周无。
▲9、补充检验方法信息:本周无。
☆三、CDE药品技术指导原则、指南发布类征求类:
◆1、关于药审中心与中国药品监督管理研究会合作举办“创新药物临床研发在不同适应症领域的审评考虑”线上培训的通知
◆2、关于公开征求《抗肿瘤抗体偶联药物临床研发技术指导原则》意见的通知
☆四、CDE新承办信息公示类
■1、境内企业新药申报承办情况统计
■2、进口申报承办情况统计:
■3、境内企业仿制药申报承办情况统计:
■4、化药一致性评价申报承办情况统计:
□(1)国内未改变处方工艺的一致性评价申请或提出免于参加一致性评价的申请:
□(2)进口未改变处方工艺的一致性评价申请或提出免于参加一致性评价的申请:本周无。
□(3)国内改变处方工艺的一致性评价:
□(4)进口改变处方工艺的一致性评价:本周无。
■5、原料药登记信息公示:
■6、药用辅料登记信息公示:
■7、药包材登记信息公示:
☆五、CDE信息公示类
●1、临床试验默示许可:新增59条,共计8134条
●2、优先审评公示
○(1)拟优先审评品种公示:伯瑞替尼肠溶胶囊
○(2)纳入优先审评品种:本周无。
○(3)异议论证结果查询:本周无。
●3、突破性治疗公示
○(1)拟突破性治疗品种公示:本周无。
○(2)纳入突破性治疗品种:CMG901、YK-029A片
○(3)异议论证结果查询:本周无。
●4、《化学仿制药参比制剂目录》的公示:本周无新增,公示共计六十二批
●5、共性问题:
○(1)受理共性问题:本周无新增,共计36条
○(2)常见一般性技术问题:本周无新增,共计144条
●6、仿制药质量和疗效一致性评价百问百答:本周无新增,共计3期41个问答
●7、eCTD专栏 >> 常见问答:本周无新增,共计10条
●8、上市药品信息:新增7条,涉及6个品种为:环泊酚注射液、注射用亚锡替曲膦、乌帕替尼缓释片、阿立哌唑口溶膜、度伐利尤单抗注射液、特立帕肽注射液,信息公示共计966条
○(1)2022年09月13日:新增1条,涉及1个品种为:环泊酚注射液
○(2)2022年09月14日:新增1条,涉及1个品种为:注射用亚锡替曲膦
○(3)2022年09月15日:新增4条,涉及3个品种为:乌帕替尼缓释片、阿立哌唑口溶膜、度伐利尤单抗注射液
○(4)2022年09月16日:新增1条,涉及1个品种为:特立帕肽注射液
☆六、CMDE发布公示信息:
∮国家药监局器审中心关于发布纤维蛋白单体测定试剂等27项医疗器械产品注册审查指导原则的通告(2022年第35号)
∮关于公开征求《眼科光学测量设备注册审查指导原则(征求意见稿)》意见的通知
☆七、NMPAIC发布公示信息:本周无。
☆八、CFDI发布公示信息:
¢关于延期举办2022年第二期药物临床试验注册核查交流会的通知
¢关于公开征求《血液制品生产现场检查指南(征求意见稿)》意见的通知
☆九、CHP发布公示信息:
⊙关于公开征求《化学药品通用名称命名指导原则》意见的函
⊙关于举办《中国药典》生物制品质量控制专项线上培训班的通知
⊙关于再次延期举办《中国药典》药物制剂质量控制技术研讨培训的通知
⊙标准公示——胰酶胆汁肠溶片(曾用名:复方胰酶片)、多潘立酮片(第二次)、蚓激酶肠溶片、蚓激酶、蚓激酶肠溶胶囊国家药品标准草案的公示、三氯叔丁醇药用辅料标准草案的公示
☆十、NIFDC发布公示信息:
◎中国食品药品检定研究院2023年硕士研究生招生简章
☆十一、CDR-ADR发布公示信息:本周无。
☆十二、CFE-SAMR发布公示信息:本周无。
☆十三、CNCSDR发布公示信息:
¤创新药及罕见病药物研发技术指导原则培训会在线举办
¤关于召开药品政策法规宣讲基层行——创新药在不同适应症下的审评考虑线上培训会通知
☆一、NMPA政策文件发布征求类:
★1、国家药监局关于批准注册210个医疗器械产品公告 (2022年8月) (2022年第78号)
链接:
https://www.nmpa.gov.cn/xxgk/ggtg/ylqxpzhzhcchpgg/20220916144510121.html

★2、国家药监局关于17批次药品不符合规定的通告(2022年第43号)
链接:
https://www.nmpa.gov.cn/xxgk/ggtg/ypchj/ypgjjgg/20220915171443184.html

☆二、NMPA信息公示类
▲1、上市批准信息公示:
△新药上市批准信息公示:广金钱草总黄酮胶囊
△新医疗器械上市批准信息公示:本周无。
△其他上市信息公示:本周无。
▲2、仿制药参比制剂目录发布信息:本周新增第五十八批,共计发布五十八批。

链接:
https://www.nmpa.gov.cn/xxgk/ggtg/qtggtg/20220914152446193.html

▲3、说明书修订信息:本周无。
▲4、药品批准证明文件待领取信息发布:
△2022年9月15日

▲5、药品通知件待领取信息发布:
△2022年9月14日
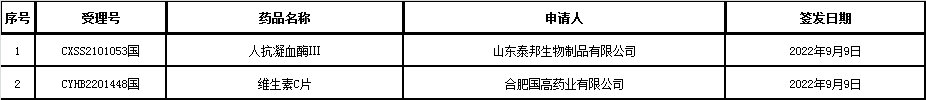
▲6、药品批准证明文件(纠错)待领取信息:本周无。
▲7、中药品种保护信息公示:本周无。
▲8、药品注册证书注销、暂停进口信息:本周无。
▲9、补充检验方法信息:本周无。
☆三、CDE药品技术指导原则、指南发布类征求类:
◆1、关于药审中心与中国药品监督管理研究会合作举办“创新药物临床研发在不同适应症领域的审评考虑”线上培训的通知
链接:
https://www.cde.org.cn/main/news/viewInfoCommon/64dd6e9a46d87904062753a950313772

◆2、关于公开征求《抗肿瘤抗体偶联药物临床研发技术指导原则》意见的通知
链接:
https://www.cde.org.cn/main/news/viewInfoCommon/0e75a9912c9673e43cff1fa2b94f057c

☆四、CDE新承办信息公示类
■1、境内企业新药申报承办情况统计
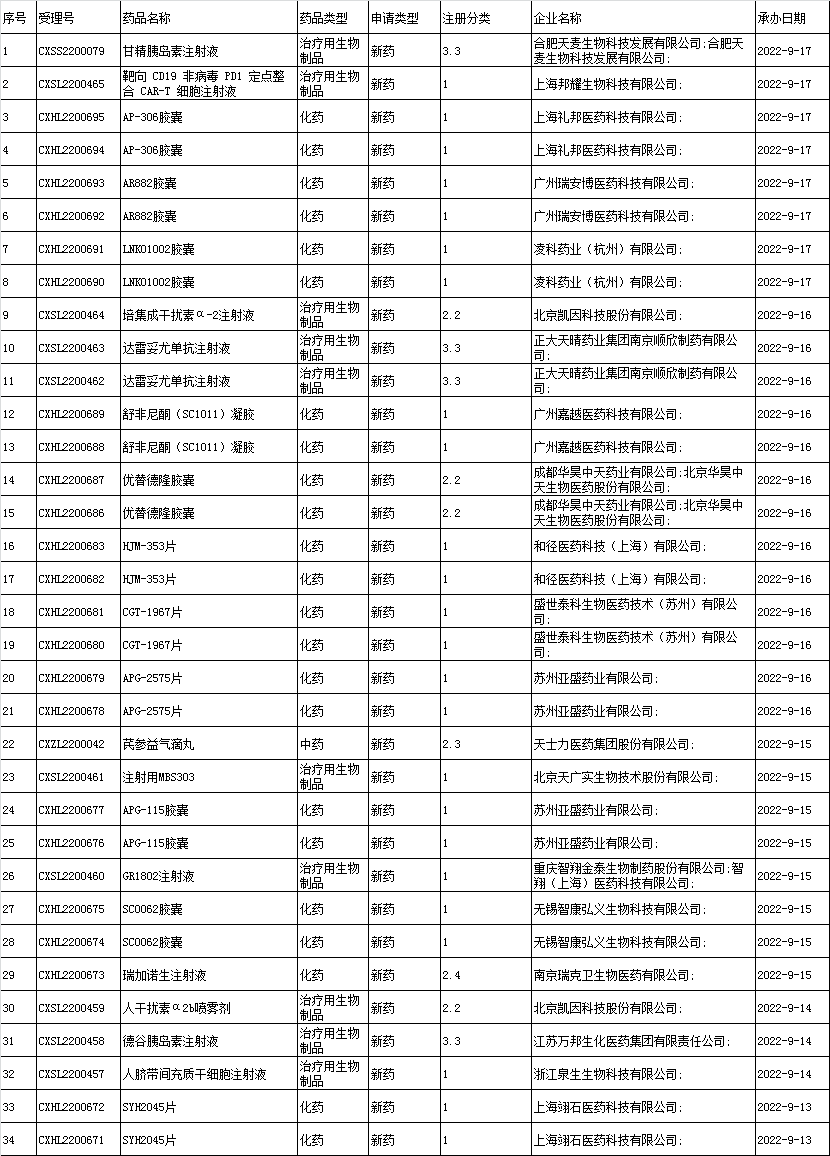
■2、进口申报承办情况统计:
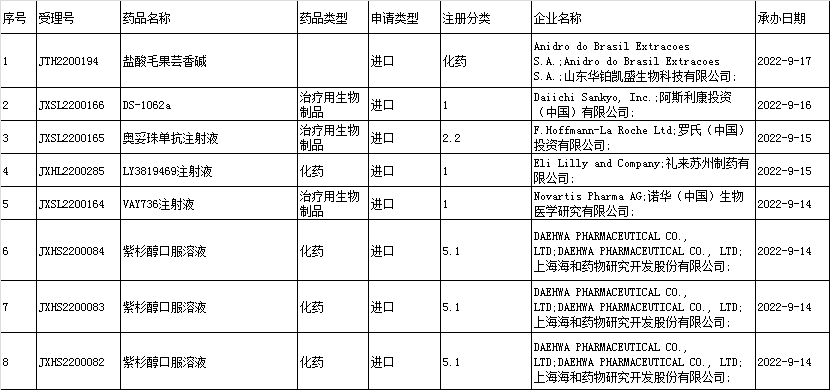
■3、境内企业仿制药申报承办情况统计:
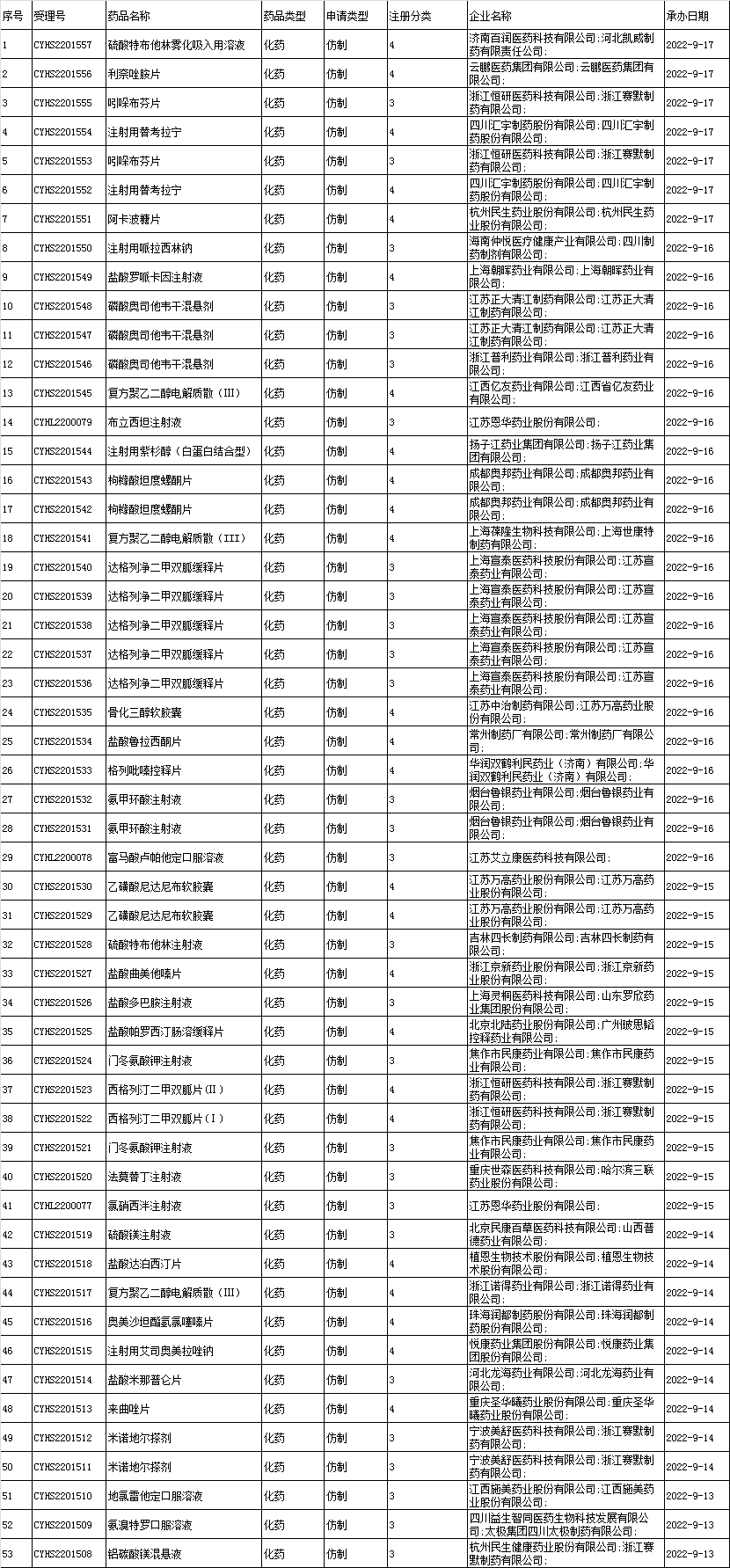
■4、化药一致性评价申报承办情况统计:
□(1)国内未改变处方工艺的一致性评价申请或提出免于参加一致性评价的申请:

□(2)进口未改变处方工艺的一致性评价申请或提出免于参加一致性评价的申请:本周无。
□(3)国内改变处方工艺的一致性评价:
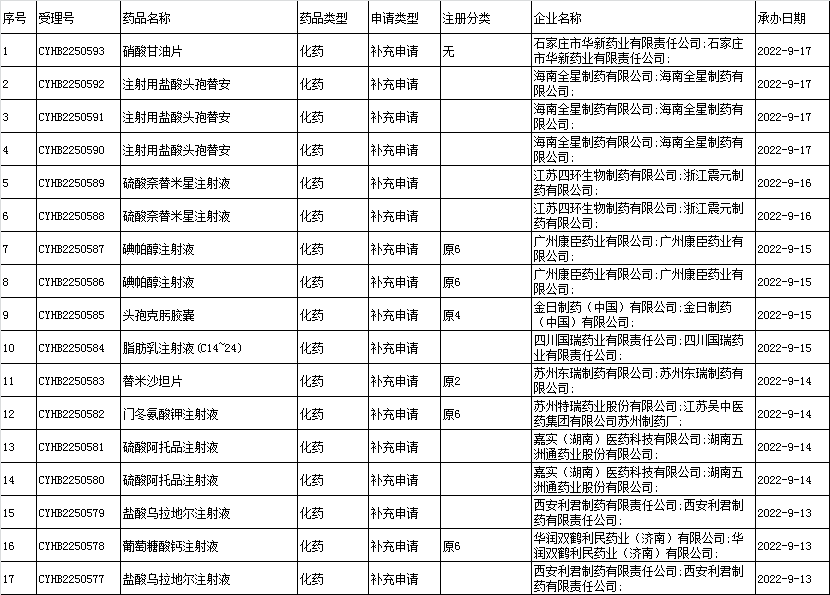
□(4)进口改变处方工艺的一致性评价:本周无。
■5、原料药登记信息公示:

■6、药用辅料登记信息公示:
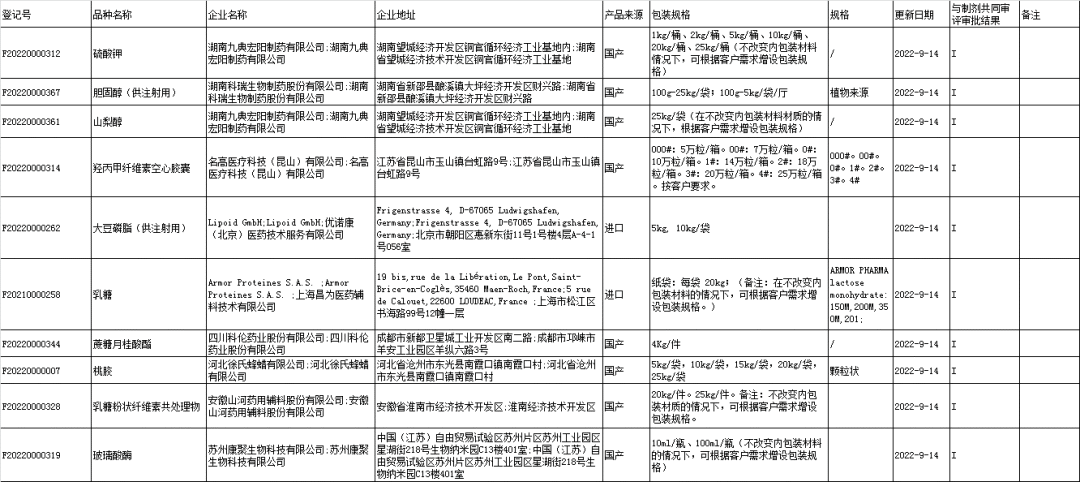
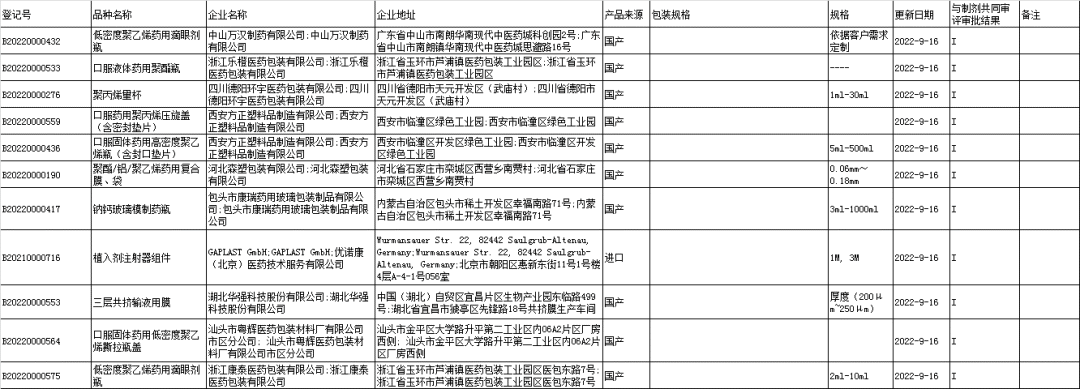
■7、药包材登记信息公示:
☆五、CDE信息公示类
●1、临床试验默示许可:新增59条,共计8134条

●2、优先审评公示
○(1)拟优先审评品种公示:伯瑞替尼肠溶胶囊


○(2)纳入优先审评品种:本周无。
○(3)异议论证结果查询:本周无。
●3、突破性治疗公示
○(1)拟突破性治疗品种公示:本周无。
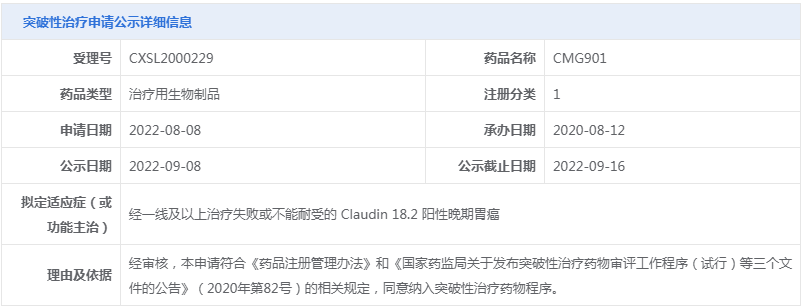
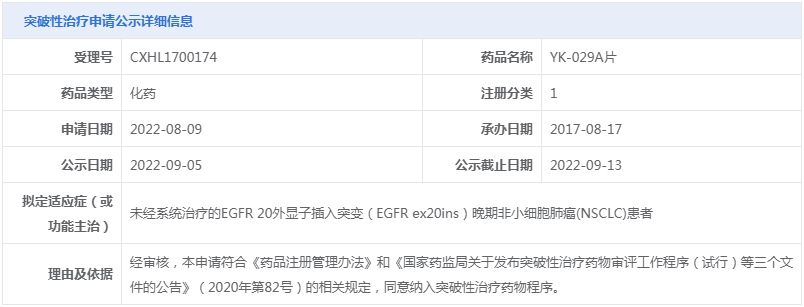
○(2)纳入突破性治疗品种:CMG901、YK-029A片

○(3)异议论证结果查询:本周无。
●4、《化学仿制药参比制剂目录》的公示:本周无新增,公示共计六十二批
●5、共性问题:
○(1)受理共性问题:本周无新增,共计36条
○(2)常见一般性技术问题:本周无新增,共计144条
●6、仿制药质量和疗效一致性评价百问百答:本周无新增,共计3期41个问答
●7、eCTD专栏 >> 常见问答:本周无新增,共计10条
●8、上市药品信息:新增7条,涉及6个品种为:环泊酚注射液、注射用亚锡替曲膦、乌帕替尼缓释片、阿立哌唑口溶膜、度伐利尤单抗注射液、特立帕肽注射液,信息公示共计966条
○(1)2022年09月13日:新增1条,涉及1个品种为:环泊酚注射液

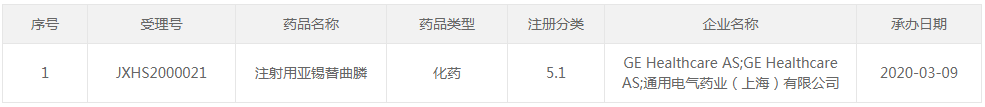
○(2)2022年09月14日:新增1条,涉及1个品种为:注射用亚锡替曲膦
○(3)2022年09月15日:新增4条,涉及3个品种为:乌帕替尼缓释片、阿立哌唑口溶膜、度伐利尤单抗注射液

○(4)2022年09月16日:新增1条,涉及1个品种为:特立帕肽注射液

☆六、CMDE发布公示信息:
∮国家药监局器审中心关于发布纤维蛋白单体测定试剂等27项医疗器械产品注册审查指导原则的通告(2022年第35号)

链接:
https://www.cmde.org.cn/xwdt/zxyw/20220915161228148.html

∮关于公开征求《眼科光学测量设备注册审查指导原则(征求意见稿)》意见的通知
链接:
https://www.cmde.org.cn/xwdt/zxyw/20220913133433136.html

☆七、NMPAIC发布公示信息:本周无。
☆八、CFDI发布公示信息:
¢关于延期举办2022年第二期药物临床试验注册核查交流会的通知
链接:
https://www.cfdi.org.cn/resource/news/14821.html

¢关于公开征求《血液制品生产现场检查指南(征求意见稿)》意见的通知
链接:
https://www.cfdi.org.cn/resource/news/14816.html

☆九、CHP发布公示信息:
⊙关于公开征求《化学药品通用名称命名指导原则》意见的函
链接:
https://www.chp.org.cn/gjyjw/tz/17275.jhtml

⊙关于举办《中国药典》生物制品质量控制专项线上培训班的通知
链接:
https://www.chp.org.cn/gjyjw/tz/17280.jhtml

⊙关于再次延期举办《中国药典》药物制剂质量控制技术研讨培训的通知
链接:
https://www.chp.org.cn/gjyjw/tz/17286.jhtml

⊙标准公示——胰酶胆汁肠溶片(曾用名:复方胰酶片)、多潘立酮片(第二次)、蚓激酶肠溶片、蚓激酶、蚓激酶肠溶胶囊国家药品标准草案的公示、三氯叔丁醇药用辅料标准草案的公示
☆十、NIFDC发布公示信息:
◎中国食品药品检定研究院2023年硕士研究生招生简章
链接:
https://www.nifdc.org.cn/nifdc/xxgk/ggtzh/yjshpy/20220915092648268534.html

☆十一、CDR-ADR发布公示信息:本周无。
☆十二、CFE-SAMR发布公示信息:本周无。
☆十三、CNCSDR发布公示信息:
¤创新药及罕见病药物研发技术指导原则培训会在线举办


¤关于召开药品政策法规宣讲基层行——创新药在不同适应症下的审评考虑线上培训会通知



链接:
https://www.cncsdr.org/ggtz/zxtz/202209/t20220916_308671.html



END

往期推荐




