国家药监局及直属单位药品相关数据信息一周集锦(2022-07-25至2022-07-30)


目录
☆一、NMPA政策文件发布征求类:
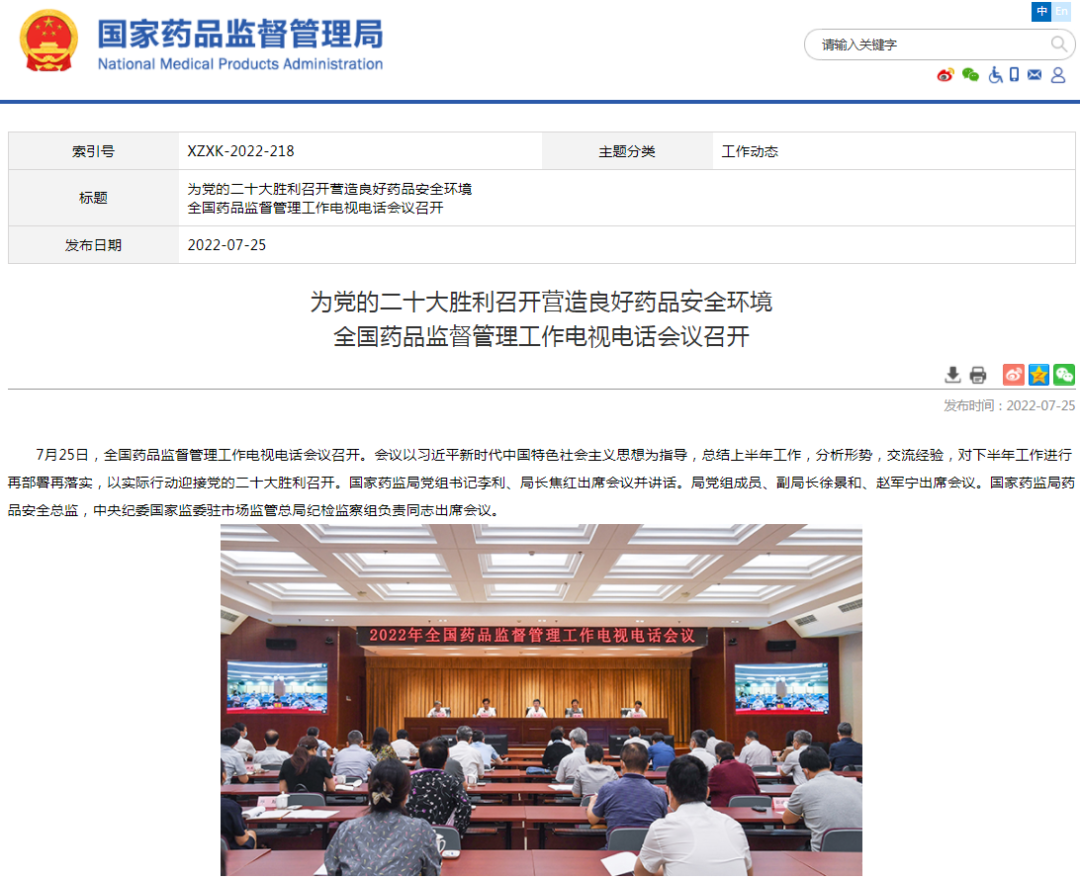
★为党的二十大胜利召开营造良好药品安全环境全国药品监督管理工作电视电话会议召开
☆二、NMPA信息公示类
▲1、上市批准信息公示:
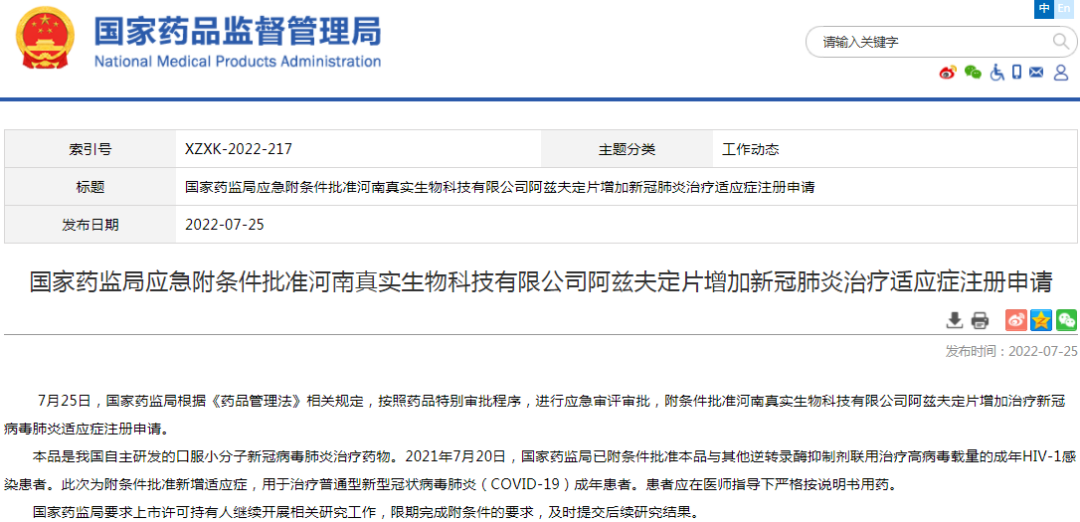
△新药上市批准信息公示:阿兹夫定片增加新冠肺炎治疗适应症
△新医疗器械上市批准信息公示:血管内超声诊断仪和一次性使用血管内超声诊断导管
△其他上市信息公示:本周无。
▲2、仿制药参比制剂目录发布信息:本周无新增,共计发布五十六批。
▲3、说明书修订信息:本周无。
▲4、药品批准证明文件待领取信息发布:
△2022年7月26日
△2022年7月29日
▲5、药品通知件待领取信息发布:
△2022年7月26日
△2022年7月29日
▲6、药品批准证明文件(纠错)待领取信息:本周无。
▲7、中药品种保护信息公示:本周无。
▲8、药品注册证书注销、暂停进口信息:本周无。
▲9、补充检验方法信息:本周无。
☆三、CDE药品技术指导原则、指南发布类征求类:
◆1、公开征求《药物临床试验盲法指导原则》意见的通知
◆2、公开征求ICH指导原则《M12:药物相互作用》意见的通知
☆四、CDE新承办信息公示类
■1、境内企业新药申报承办情况统计
■2、进口申报承办情况统计:
■3、境内企业仿制药申报承办情况统计:
■4、化药一致性评价申报承办情况统计:
□(1)国内未改变处方工艺的一致性评价申请或提出免于参加一致性评价的申请:本周无。
□(2)进口未改变处方工艺的一致性评价申请或提出免于参加一致性评价的申请:本周无。
□(3)国内改变处方工艺的一致性评价:
□(4)进口改变处方工艺的一致性评价:本周无。
■5、原料药登记信息公示:
■6、药用辅料登记信息公示:
■7、药包材登记信息公示:
☆五、CDE信息公示类
●1、临床试验默示许可:新增63条,共计7695条
●2、优先审评公示
○(1)拟优先审评品种公示:本周无。
○(2)纳入优先审评品种:注射用双羟萘酸曲普瑞林、盐酸哌甲酯缓释咀嚼片
○(3)异议论证结果查询:本周无。
●3、突破性治疗公示
○(1)拟突破性治疗品种公示:本周无。
○(2)纳入突破性治疗品种:本周无。
○(3)异议论证结果查询:本周无。
●4、《化学仿制药参比制剂目录》的公示:本周新增第六十一批,公示期限:2022年7月27日~2022年8月9日(10个工作日),公示共计六十一批
○(1)化学仿制药尚未发布参比制剂目录(第六十一批)(征求意见稿)
○(2)已发布化学仿制药参比制剂增补目录(征求意见稿)
○(3)未通过审议品种目录
○(4)再议品种目录
●5、共性问题:
○(1)受理共性问题:本周无新增,共计36条
○(2)常见一般性技术问题:本周无新增,共计144条
●6、仿制药质量和疗效一致性评价百问百答:本周无新增,共计3期41个问答
●7、eCTD专栏 >> 常见问答:本周无新增,共计10条
●8、上市药品信息:新增7条,涉及4个品种为:度恩西布胶囊、依帕伐单抗注射液,信息公示共计922条
○(1)2022年7月25日:新增5条,涉及2个品种为:度恩西布胶囊、依帕伐单抗注射液
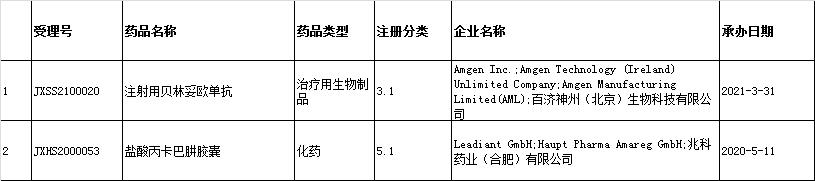
○(2)2022年7月27日:新增2条,涉及2个品种为:注射用贝林妥欧单抗、盐酸丙卡巴肼胶囊
☆六、CMDE发布公示信息:本周无。
☆七、NMPAIC发布公示信息:本周无。
☆八、CFDI发布公示信息:
¢关于2022中国制药工程大会延期的通知
☆九、CHP发布公示信息:
◎标准公示——余甘子国家药品标准草案
☆十、NIFDC发布公示信息:
∈关于启用中检院新的检验报告封二页的通知
☆十一、CDR-ADR发布公示信息:
∝关于第六届中国医疗器械警戒大会的通知 (第一轮)
☆十二、CFE-SAMR发布公示信息:本周无。
☆十三、CNCSDR发布公示信息:
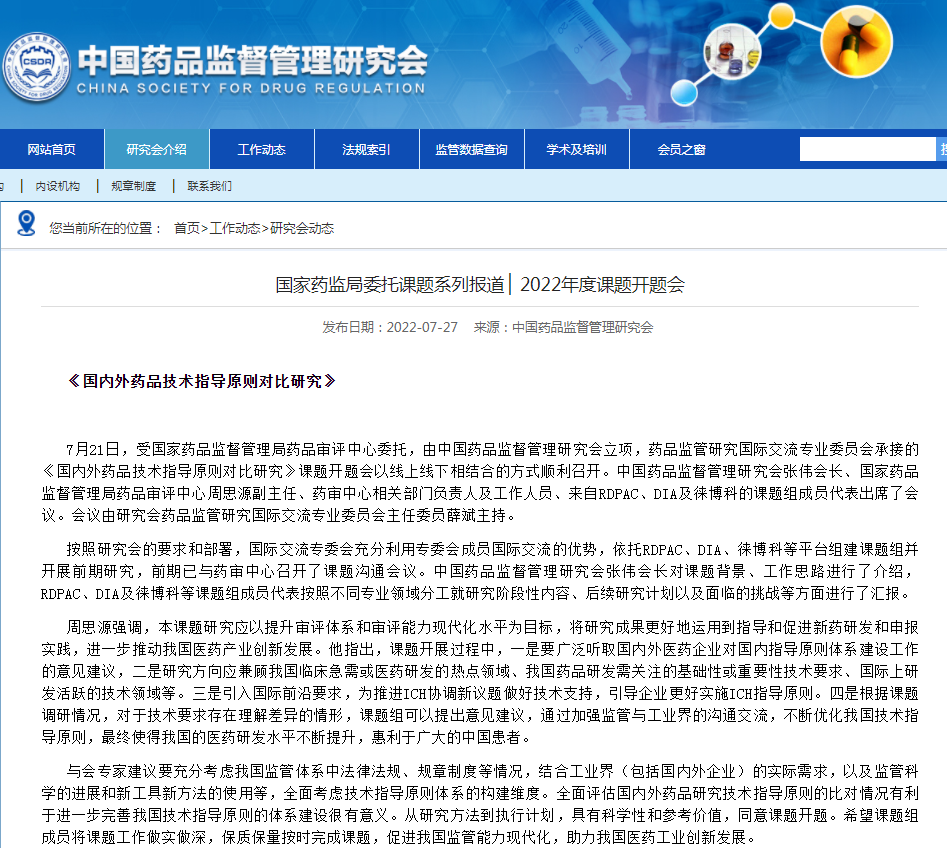
£国家药监局委托课题系列报道 ▏2022年度课题开题会
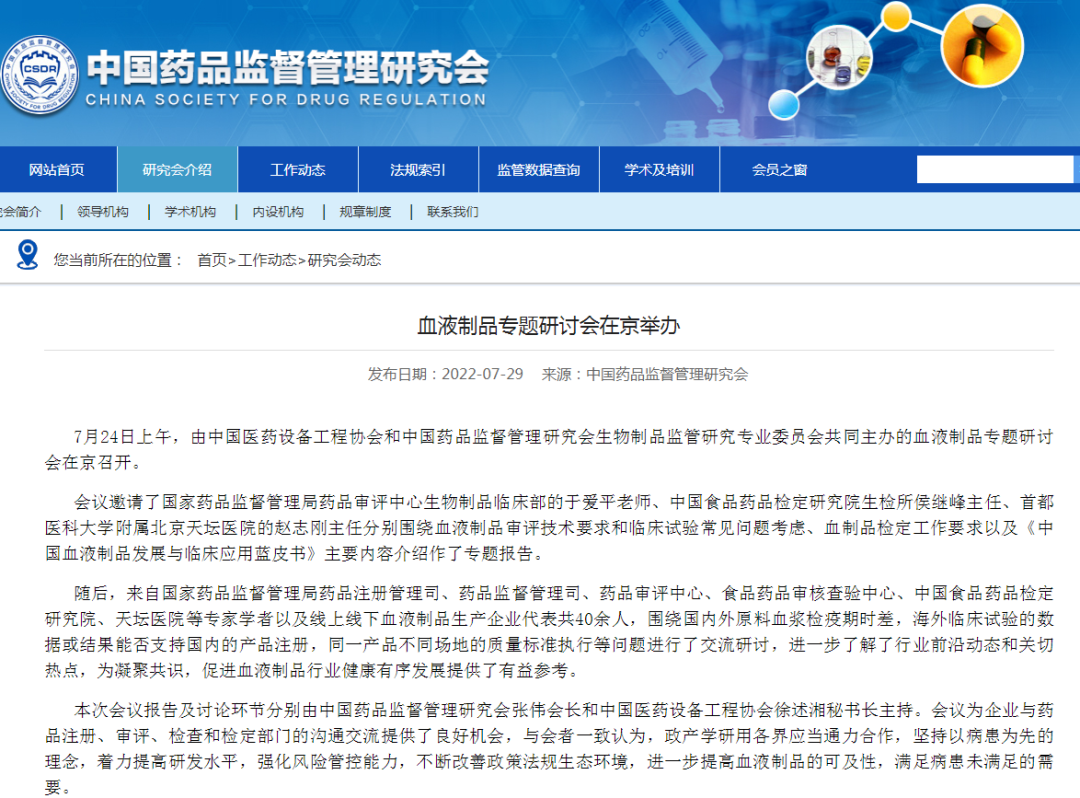
£血液制品专题研讨会在京举办

☆一、NMPA政策文件发布征求类:
★为党的二十大胜利召开营造良好药品安全环境全国药品监督管理工作电视电话会议召开

☆二、NMPA信息公示类
▲1、上市批准信息公示:
△新药上市批准信息公示:阿兹夫定片增加新冠肺炎治疗适应症
△新医疗器械上市批准信息公示:血管内超声诊断仪和一次性使用血管内超声诊断导管

△其他上市信息公示:本周无。
▲2、仿制药参比制剂目录发布信息:本周无新增,共计发布五十六批。
▲3、说明书修订信息:本周无。
▲4、药品批准证明文件待领取信息发布:
△2022年7月26日

△2022年7月29日

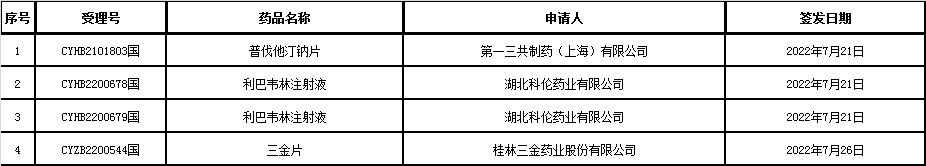
▲5、药品通知件待领取信息发布:
△2022年7月26日

△2022年7月29日
▲6、药品批准证明文件(纠错)待领取信息:本周无。
▲7、中药品种保护信息公示:本周无。
▲8、药品注册证书注销、暂停进口信息:本周无。
▲9、补充检验方法信息:本周无。
☆三、CDE药品技术指导原则、指南发布类征求类:
◆1、公开征求《药物临床试验盲法指导原则》意见的通知

链接:
https://www.cde.org.cn/main/news/viewInfoCommon/5b3876938c6381e89051509b2a301d88

◆2、公开征求ICH指导原则《M12:药物相互作用》意见的通知

链接:
https://www.cde.org.cn/main/news/viewInfoCommon/1c0776c59f4c94561c2aab3bf7b393a8

☆四、CDE新承办信息公示类
■1、境内企业新药申报承办情况统计

■2、进口申报承办情况统计:

■3、境内企业仿制药申报承办情况统计:
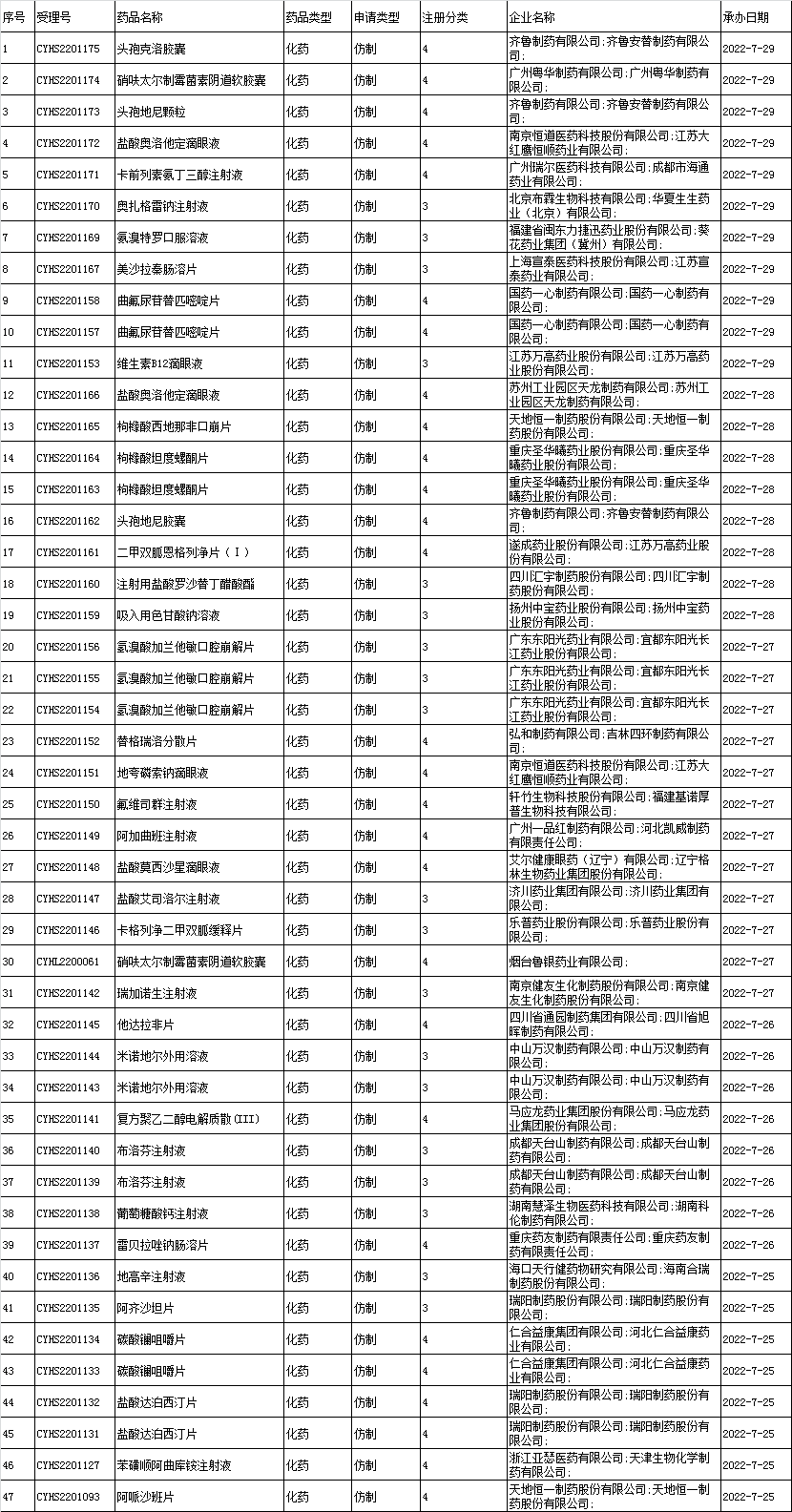
■4、化药一致性评价申报承办情况统计:
□(1)国内未改变处方工艺的一致性评价申请或提出免于参加一致性评价的申请:本周无。
□(2)进口未改变处方工艺的一致性评价申请或提出免于参加一致性评价的申请:本周无。
□(3)国内改变处方工艺的一致性评价:

□(4)进口改变处方工艺的一致性评价:本周无。
■5、原料药登记信息公示:

■6、药用辅料登记信息公示:

■7、药包材登记信息公示:

☆五、CDE信息公示类
●1、临床试验默示许可:新增63条,共计7695条

●2、优先审评公示
○(1)拟优先审评品种公示:本周无。
○(2)纳入优先审评品种:注射用双羟萘酸曲普瑞林、盐酸哌甲酯缓释咀嚼片





○(3)异议论证结果查询:本周无。
●3、突破性治疗公示
○(1)拟突破性治疗品种公示:本周无。
○(2)纳入突破性治疗品种:本周无。
○(3)异议论证结果查询:本周无。
●4、《化学仿制药参比制剂目录》的公示:本周新增第六十一批,公示期限:2022年7月27日~2022年8月9日(10个工作日),公示共计六十一批
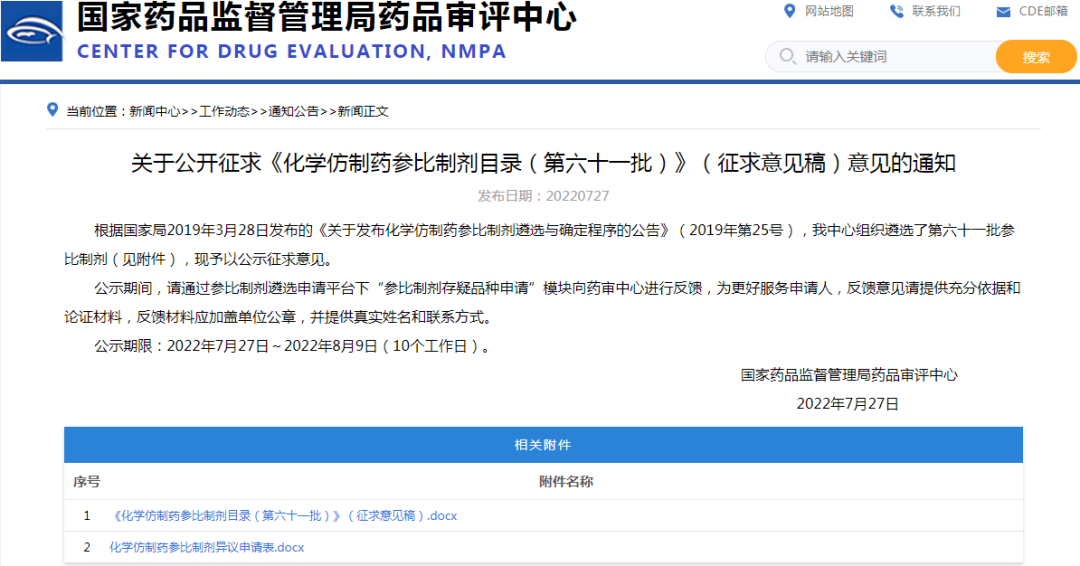
链接:
https://www.cde.org.cn/main/news/viewInfoCommon/e99c0492b135364afd06a2e38498949b

○(1)化学仿制药尚未发布参比制剂目录(第六十一批)(征求意见稿)


○(2)已发布化学仿制药参比制剂增补目录(征求意见稿)


○(3)未通过审议品种目录

○(4)再议品种目录

●5、共性问题:
○(1)受理共性问题:本周无新增,共计36条
○(2)常见一般性技术问题:本周无新增,共计144条
●6、仿制药质量和疗效一致性评价百问百答:本周无新增,共计3期41个问答
●7、eCTD专栏 >> 常见问答:本周无新增,共计10条
●8、上市药品信息:新增7条,涉及4个品种为:度恩西布胶囊、依帕伐单抗注射液,信息公示共计922条
○(1)2022年7月25日:新增5条,涉及2个品种为:度恩西布胶囊、依帕伐单抗注射液

○(2)2022年7月27日:新增2条,涉及2个品种为:注射用贝林妥欧单抗、盐酸丙卡巴肼胶囊
☆六、CMDE发布公示信息:本周无。
☆七、NMPAIC发布公示信息:本周无。
☆八、CFDI发布公示信息:
¢关于2022中国制药工程大会延期的通知
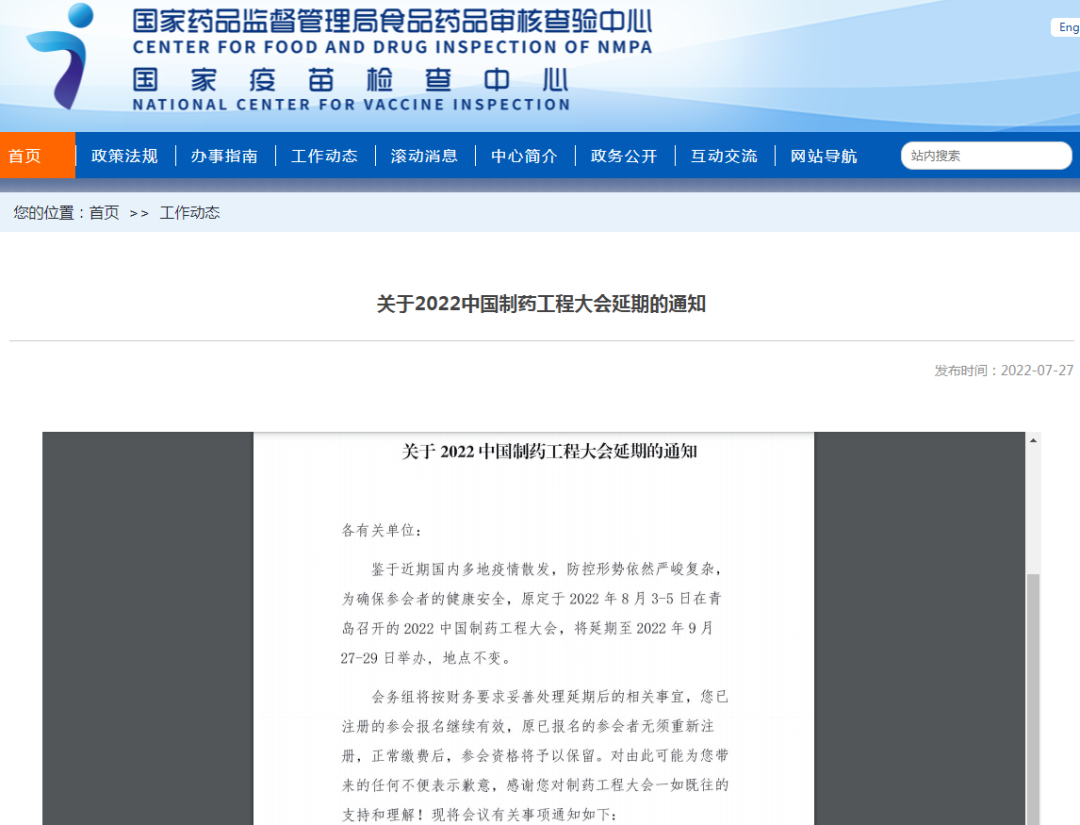
链接:
https://www.cfdi.org.cn/resource/news/14736.html

☆九、CHP发布公示信息:
◎标准公示——余甘子国家药品标准草案

☆十、NIFDC发布公示信息:
∈关于启用中检院新的检验报告封二页的通知

链接:
https://www.nifdc.org.cn/nifdc/xxgk/ggtzh/pxtzh/20220719082828191143.html

☆十一、CDR-ADR发布公示信息:
∝关于第六届中国医疗器械警戒大会的通知 (第一轮)

链接:
https://www.cdr-adr.org.cn/center_news/202207/t20220728_49777.html

☆十二、CFE-SAMR发布公示信息:本周无。
☆十三、CNCSDR发布公示信息:
£国家药监局委托课题系列报道 ▏2022年度课题开题会

£血液制品专题研讨会在京举办


精彩专题
“凝聚红色力量,践行初心使命”阳光诺庆祝建党101华诞主题活动
《药视情报站》05期-对抗“儿童杀手—ALL“,微片技术显神功





